АА-амилоидоз – это состояние, включающее внеклеточное отложение биологически неактивного белка неразветвленной структуры и бета-конфигурации, которое создает характерную гистопатологическую картину. Этот белок встречается у человека только при патологических состояниях. Заболевание является осложнением хронического воспаления, инфекций и злокачественных опухолей.
До недавнего времени АА-амилоидоз был наиболее распространенной формой системного амилоидоза в мире, но открытие новых и эффективных методов борьбы с воспалительными заболеваниями, особенно биопрепаратами, снизило заболеваемость АА-амилоидозом, по крайней мере, в западных странах.
Содержание статьи
Причины амилоидоза AA
Причины амилоидоза AA включают:
- хронические воспалительные заболевания суставов – ревматоидный артрит, ювенильный идиопатический артрит и другие артриты в 60% случаев;
- хронические инфекции – бронхоэктазы, осложнения параплегии и туберкулеза, инфицированные пролежни, хронический остеомиелит, хронические язвы ног.
- аутоиммунные воспалительные заболевания – семейная средиземноморская лихорадка с фактором некроза опухоли, TNF, рецептор-ассоциированный рецидивирующий синдром, синдром Макл-Уэллса, гипер-IgD и синдром перемежающейся лихорадки – 9% случаев;
- болезнь Крона – 5%;
- следствие злокачественных опухолей, когда они продуцируют провоспалительные цитокины, например, при раке почки, – у 3% пациентов;
- другие причины – синдром Кастельмана, опухоли, васкулит в 6% случаев;
- неизвестные (неустановленные) причины – 6% случаев.
При отсутствии сопутствующих заболеваний следует учитывать генетическую основу амилоидоза, включая мутацию белка SAA4.
Патологический амилоидный белок AA во время амилоидоза образуется из N-концевых фрагментов реактивного воспалительного белка SAA, продуцируемого в печени. Производство белка SAA в печени активируется системными воспалительными цитокинами, выделяемыми во время воспаления.
АА амилоидоз обычно включает поражение почек, печени и селезенки, поскольку именно там чаще всего откладывается амилоидный белок, а течение и клинические симптомы заболевания определяются поражением почек, которое осложняется протеинурией и почечной недостаточностью. TIFN развивается у 40%. пациентов. Установлена связь между уровнем белка SAA в крови и функцией почек, повреждением органов, вызванным амилоидом, и смертностью пациентов.
Эпидемиология
Существуют значительные различия в заболеваемости амилоидозом АА в разных странах. Причина этого явления – помимо переменной частоты заболеваний, приводящих к амилоидозу AA, — также в другой генетической предрасположенности (аллель SAA1). Амилоидоз АА чаще диагностируется в Европе, чем в США.
Эпидемиология амилоидоза АА окончательно не определена и основана на данных аутопсии. Подсчитано, что в западных странах заболеваемость колеблется от 0,5% до 21,4% и зависит от факторов риска окружающей среды и генетической предрасположенности. По данным из Испании, амилоидоз АА при биопсии почки обнаруживают у 4% больных, а в Италии – у 2,5%.
С учетом некоторых причин амилоидоза АА он обнаруживается:
- у 37% больных семейной средиземноморской лихорадкой;
- у 17% больных туберкулезом;
- у 7–29% больных ревматоидным артритом;
- у 7–21,4% больных анкилозирующим спондилитом.
Бытует мнение, что частота амилоидоза снижается (особенно в сравнительных финских исследованиях). Количество биопсий, выполняемых для поиска амилоидных отложений, также уменьшается. Поэтому неизвестно, имеем ли мы дело с реальным снижением частоты амилоидоза или снижением диагностической настороженности ревматологов (или клиническая картина стала менее типичной).
Более низкая заболеваемость амилоидозом в западных странах скорее всего связана с контролем над эпидемией туберкулеза и остеомиелита. Также способствует снижению вторичного амилоидоза раннее использование лекарств, модифицирующих заболевание.
Патофизиология
Существует более 25 различных белков, которые имеют тенденцию объединяться под влиянием других факторов. Это приводит к образованию волокон с характерной конфигурацией, состоящих из четырех-шести протофиламентов, скрученных друг вокруг друга.
Фибриллы амилоида A образуются из сывороточного амилоида A (SAA – сывороточный амилоид A). SAA – это белок острой фазы, входящий в состав липопротеинов высокой плотности (HDL), синтезируемый в печени под действием провоспалительных цитокинов (интерлейкин 1, интерлейкин 6, TNF).
Средняя нормальная концентрация SAA в крови составляет 3 мг/л. Под влиянием инфекции она может повышаться до более 1000–2000 мг/л в течение 24–48 часов. При хронических воспалительных процессах концентрация постоянно повышается. В результате ферментативной деградации лизосомальной протеазой первые 76 из 104 аминокислот отделяются и образуется амилоидный белок А. Предполагается, что также участвуют в этой трансформации тучные клетки.
Амилоидные отложения также включают:
- амилоидный белок P
- протеогликаны, такие как гепарансульфат
- гликозаминогликаны
- компоненты дополнения
- и ApoE.
Фактор, усиливающий образование амилоида
В образовании амилоидных фибрилл, которые образуются в ретикулоэндотелиальной системе печени и селезенки при длительном воспалении, участвует фактор усиления амилоида (AEF). Этот фактор можно сравнить с ядром, вокруг которого начинается образование амилоидных волокон.
Образование амилоидных отложений
Во-первых, считается, что физиологический ответ на воспалительный фактор вызывает значительное количество ААС. Затем из-за физиологической роли ААС в метаболизме ЛПВП при воспалении его пул смещается в места скопления макрофагов. Там при участии фактора, способствующего образованию амилоида, чрезмерное накопление амилоида происходит позже.
Амилоидные отложения динамически восстанавливаются в зависимости, например, от концентрации SAA в плазме. Они защищены от протеолиза гликозаминогликанами и амилоидным белком P. Процесс амилоидогенеза не обязательно должен быть необратимым, поскольку при снижении концентрации SAA в плазме иногда наблюдается регресс амилоидных отложений.
Клиническая картина амилоидоза АА
Общие симптомы амилоидоза включают:
- потерю веса;
- усталость;
- слабость.
Остальные симптомы возникают в результате поражения отдельных органов.
Симптомы поражения органов
- Нефропатия. Амилоидные отложения могут накапливаться по всему телу. Однако наибольшее клиническое значение имеет их накопление в почках и вызываемая ими нефропатия. Амилоид может накапливаться в клубочках или в трубках, интерстиции и сосудах. Поразительно, но также трудно объяснить, но не удалось подтвердить связь между размером отложений амилоида и тяжестью заболевания. Существенных различий в параметрах липидного обмена между нефротическим синдромом, вызванным амилоидозом, и другими причинами нефроза нет.
- Гломерулярный амилоидоз. Вначале он может протекать бессимптомно, затем следует протеинурия, гипоальбуминемия и нефротический синдром с отеком конечностей. Есть особенности хронического заболевания почек.
- Тубулярный, интерстициальный и сосудистый амилоидоз. Когда амилоид откладывается в основном в канальцах и интерстициальной ткани или сосудах, протеинурия незначительна. Напротив, снижение клубочковой фильтрации находится на переднем плане. Затем ухудшение функции почек прогрессирует медленнее, чем в случае гломерулярных изменений. Артериальная гипертензия появляется при поражении сосудов. Существует корреляция между протеинурией и тяжестью тубулоинтерстициальных поражений.
- Амилоидоз желудочно-кишечного тракта. При амилоидозе возможно поражение стенки кровеносных сосудов желудочно-кишечного тракта, что приводит к инфекции, перфорации или опасному для жизни кишечному кровотечению. Основная причина кровотечения – нарушение эластичности кровеносных сосудов, вызванное отложениями амилоида. Другие симптомы включают чередование запоров и диареи, а также нарушение всасывания.
- Амилоидоз печени и селезенки. Иногда наблюдается увеличение печени и селезенки, вызывающее боли в правом и левом подреберье. Кроме того, могут возникать изъязвления и кровотечения из желудочно-кишечного тракта, а относительно редко – его непроходимость.
- Невропатия. Другие симптомы включают вегетативную невропатию, вызывающую ортостатическую гипотензию или импотенцию. Проникновение вегетативной системы также может вызвать изменения в пищеварительном тракте.
- Надпочечниковая недостаточность. Может возникнуть недостаточность коры и мозгового вещества надпочечников, вызванная инфильтрацией отложений амилоида.
Вовлечение других органов. При амилоидозе АА органы над диафрагмой поражены реже, чем органы, расположенные ниже. Когда отложения амилоида накапливаются в сердце, развивается рестриктивная кардиомиопатия и склонность к аритмиям. Узелки в легких могут возникать при поражении легких. Кроме того, наблюдается зоб, вызванный амилоидозом AA, который может быть первым симптомом заболевания.

Также описаны коагулопатии, связанные с дефицитом факторов свертывания плазмы: II, V, VII, IX и связанные с сосудистыми нарушениями, а также дисфибриногенемия. Иногда амилоидные отложения принимают форму узелков на коже конечностей.
Диагностика амилоидоза
Возможность развития амилоидоза АА необходимо учитывать у пациентов с хроническими воспалительными заболеваниями.
Важные признаки:
- длительное повышение СОЭ;
- повышение уровня CRP;
- повышение концентрации α 2-глобулина;
- снижение концентрации альбумина.
Клинического бессимптомного амилоидоза не существует, обнаружить отложения амилоида можно, например, с помощью биопсии (например, из жировой ткани).
Диагноз амилоидоза основан на гистопатологическом исследовании отложений амилоида в тканях. Показания к биопсии (жировой ткани,почек или подслизистой основы желудочно-кишечного тракта) у людей с заболеваниями, предрасполагающими к амилоидозу:
- появление протеинурии;
- повышение уровня креатинина.
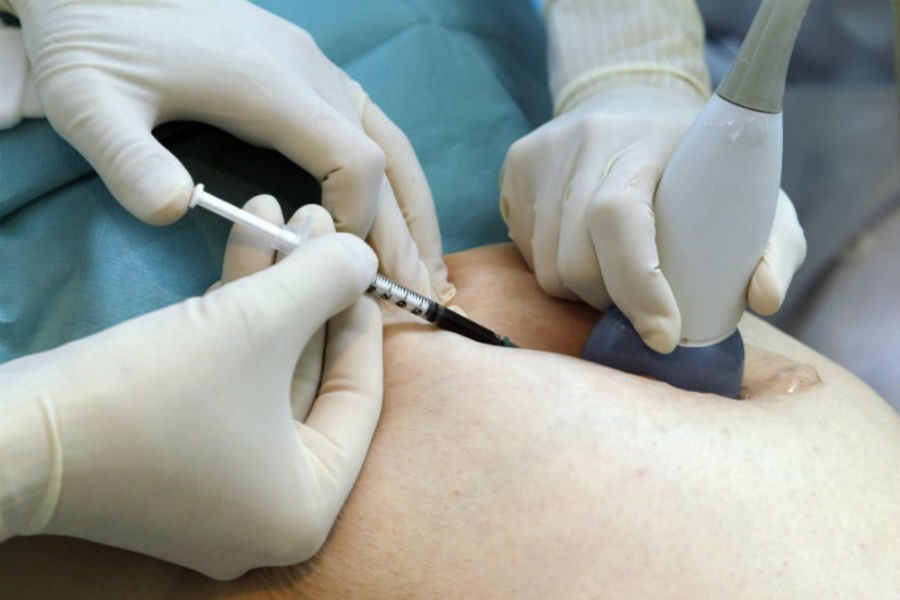
Аспирационная биопсия брюшной полости – наименее инвазивный метод получения материала для гистопатологического исследования. Он прост и безопасен, а его чувствительность при диагностике амилоидоза АА оценивается в 65-75%. При семейном амилоидозе чувствительность этого теста ниже.
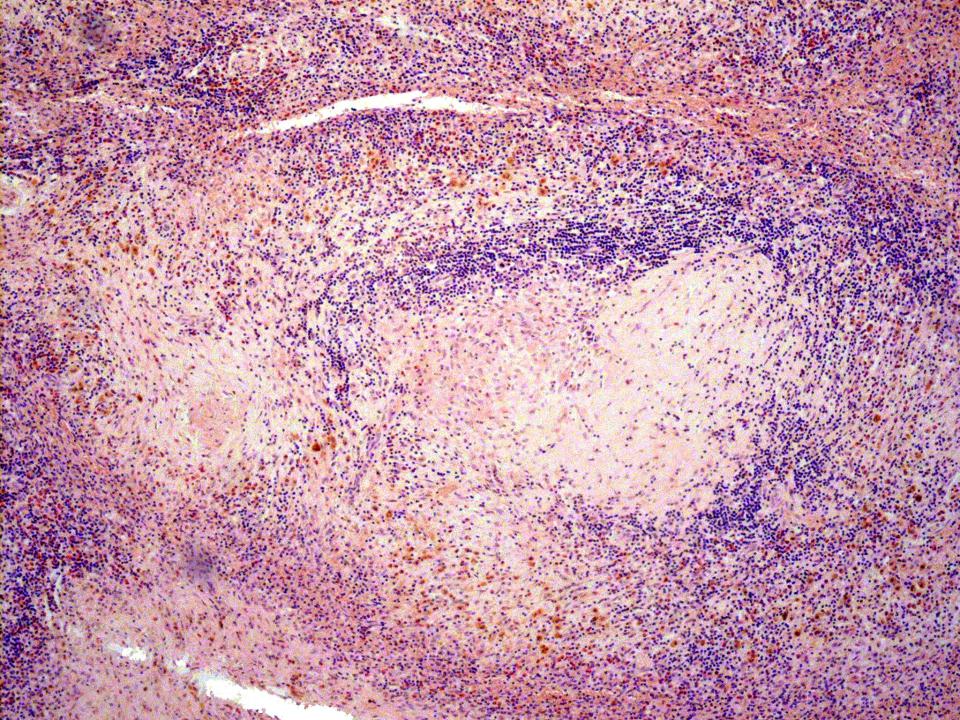
В жировой ткани отложения амилоида располагаются вокруг адипоцитов и в стенках кровеносных сосудов.
Гистологический материал окрашивают конго красным и просматривают под световым микроскопом. Амилоидные отложения становятся красными и проявляют двойное лучепреломление, которое вызывает изменение цвета в поляризованном свете на зеленый (так называемый яблочно-зеленый).
Наличие по крайней мере 3 очагов двойного лучепреломления амилоида яблочно-зеленого цвета позволяет проводить гистопатологический диагноз амилоидоза. Когда таких очагов меньше трех, результат считается слабо положительным. Причиной ложноположительных результатов может быть примесь крови, которая также дает яблочно-зеленый цвет в поляризованном свете.
Окрашивание конго красным характерно для всех типов амилоида и не позволяет дифференцировать тип амилоидоза.
Альтернативные методы получения материала включают биопсию:
- слизистой или подслизистой;
- десен;
- желудка;
- кишечника;
- ануса;
- почки;
- костного мозга.
Окрашивание конго красным не является стандартным в гистопатологии исследований тканей, кроме жировой ткани. В таких случаях, если нет признаков амилоидоза, болезнь можно не заметить.
По данным регистра при биопсии почек амилоидные отложения обнаруживаются примерно в 5% случаев. Амилоидные отложения можно обнаружить в любой части почки, но чаще всего они обнаруживаются в клубочках (аморфный материал в мезангиуме и петлях капилляров). Если бляшка присутствует в интерстициальной ткани, обнаруживается атрофия канальцев и интерстициальный фиброз.
Убедительных доказательств того, что люди с амилоидозом подвергаются большему риску кровотечения при биопсии почки, чем люди с другими заболеваниями почек, нет.
Амилоидные волокна можно увидеть с помощью электронной микроскопии, которая часто используется для оценки гистологии почек. Наличие характерных фибрилл должно быть показанием к окрашиванию образца биопсии почки Конго красным. Иногда амилоидные волокна остаются незамеченными, что приводит к ошибочной диагностике болезни почек с минимальным поражением.
Оценка поражения органов
Для оценки степени изменений органов при амилоидозе назначается сцинтиграфия с введением сывороточного амилоида P (SAP – сывороточный амилоид P). Тест состоит из введения SAP, меченного йодом 123, и получения снимков с помощью гамма-камеры. Элемент имеет способность связываться со всеми типами амилоида.
Визуальные исследования не имеют большого значения для диагностики локализации отложений белка в почках, поскольку у большинства пациентов изменений размера и структуры почек не наблюдается.
Дифференциация видов амилоидоза
Следует учитывать другие типы амилоидоза, кроме АА, из которых наиболее важными являются:
- наследственные амилоидозы;
- AL амилоидоз;
- β 2 -микроглобулин-связанный амилоидоз;
- старческий амилоидоз сердца.
Осложнения амилоидоза АА
Наиболее частые причины смерти – инфекции и хроническая почечная недостаточность, реже пациенты умирают от желудочно-кишечных кровотечений или хронической сердечной недостаточности. До внедрения в лечение биологических препаратов и метотрексата при ювенильном идиопатическом артрите амилоидоз был причиной более половины случаев смерти пациентов.
Современное лечение и перспективы лечения амилоидоза AA
Общепризнанного лечения амилоидоза АА не существует. ечение основано на уменьшении тяжести воспалительного процесса, вызванного основным заболеванием, и минимизации уровней белков острой фазы с помощью лекарств, которые изменяют основное заболевание или ингибируют активность TNF. В случае поражения органов может применяться симптоматическое лечение.
Применяются:
- стероиды, модифицирующие болезнь и биопрепараты, особенно препараты против TNF, при лечении хронического воспаления суставов;
- антибиотики при лечении хронических инфекционных заболеваний;
- колхицин и интерлейкин (IL) – колхицин уменьшает воспаление и степень амилоидных отложений в почках у пациентов с семейной средиземноморской лихорадкой и амилоидозом AA.
- антагонисты рецептора 1 при лечении препаратами против TNF и антагонисты рецептора IL-1 при лечении аутоиммунных воспалительных синдромов.
Нормализация уровней SAA в крови приводит к медленной регрессии амилоида, снижению протеинурии, улучшению почечной функции и увеличению выживаемости пациентов. Эффект лечения оценивается путем повторного тестирования уровней SAA в крови и мониторинга биологических маркеров, отражающих почечную недостаточность (24-часовая экскреция с мочой альбумина и креатинина).
Если невозможно оценить концентрацию SAA, активность заболевания можно контролировать, измеряя уровни С-реактивного белка (CRB).
Пациентам с амилоидозом AA и TIFN может выполняться трансплантация почки, но этих больных следует тщательно контролировать на предмет возможных сердечно-сосудистых и инфекционных осложнений. Рецидив амилоидоза в пересаженной почке встречается редко (4–14% пациентов). Из 59 реципиентов почек с амилоидозом AA по крайней мере одна бактериальная или условно-патогенная инфекция произошла у 73% пациентов, и общая выживаемость этих субъектов через 5 и 10 лет была хуже, чем у 177 реципиентов почек, перенесших трансплантацию почки по другой причине.
Если трансплантация почки проводится пациенту с амилоидозом AA, у которого развивается семейная средиземноморская лихорадка, поддерживающую терапию колхицином следует продолжить.
Эпродисат – это отрицательно заряженное низкомолекулярное вещество со структурой, аналогичной сульфату гепарина. Он конкурентно связывается с участками связывания гликозаминовых гликанов на белке SAA. Исследования на мышах показали, что поляризация фибрилл и, следовательно, образование амилоида ингибируется связыванием эпродизата с SAA.
Данные клинических исследований фазы 2 и 3 с участием 180 пациентов показали, что лечение амилоидозом AA в течение 2 лет у пациентов с амилоидозом AA замедляло прогрессирование заболевания и не ухудшалось так быстро, как эпродизат (800-2400 мг / день с поправкой на клиренс креатинина), функцию почек, но значительного влияния препарата на протеинурию или выживаемость выявлено не было. Исследования эффективности препарата в настоящее время продолжаются.
Продолжение статьи
- Часть 1. Системный AL амилоидоз.
- Часть 2. Амилоидоз АА – современное лечение.
- Часть 3. АТТR амилоидоз – перспективы лечения.





Для отправки комментария необходимо войти на сайт.